teoría de las colisiones:
La teoría de las colisiones propuesta por Max Trautz y William Lewis en 1916 y 1918, cualitativamente explica como reacciones químicas ocurren y porque las tasas de reacción difieren para diferentes reacciones.
Esta teoría está basada en la idea que partículas reactivas deben colisionar para que una reacción ocurra, pero solamente una cierta fracción del total de colisiones tiene la energía para conectarse efectivamente y causar transformaciones de los reactivos en productos. Esto es porque solamente una porción de las moléculas tiene energía suficiente y la orientación adecuada (o ángulo) en el momento del impacto para romper cualquier enlace existente y formar nuevas.
La cantidad mínima de energía necesaria para que esto suceda es conocida como energía de activación.
Partículas de diferentes elementos reaccionan con otras por presentar energía de activación con que aciertan las otras. Si los elementos reaccionan con otros, la colisión es llamada de suceso, pero si la concentración de al menos uno de los elementos es muy baja, habrá menos partículas para otros elementos reaccionar con aquellos y la reacción irá a suceder mucho más lentamente.
Con la temperatura aumentando, la energía cinética media y velocidad de las moléculas aumenta, pero esto es poco significativo en el aumento en el número de colisiones.
La tasa de reacción aumenta con la disminución de la temperatura porque una mayor fracción de las colisiones sobrepasa la energía de activación.
La teoría de las colisiones está íntimamente relacionada a la cinética química.
Los átomos de las moléculas de los reactivos están siempre en movimiento, generando muchas colisiones (choques). Parte de estas colisiones aumentan la velocidad de reacción química. Cuantos más choques con energía y geometría adecuada exista, mayor la velocidad de la reacción.
Hay dos tipos de colisiones:
- Horizontal – Colisión más lenta
- Vertical – Colisión más rápida, colisión efectiva
Veamos los dos modelos de colisiones para la formación de dos moléculas de HCl:
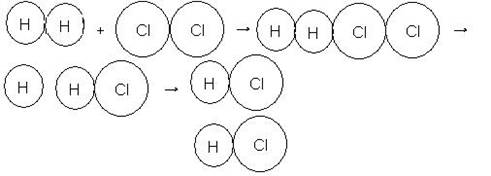
Colisión Horizontal:
Observemos que luego de la primer colisión existe formación de apenas una molécula de HCl. La segunda molécula se formará en la segunda colisión.
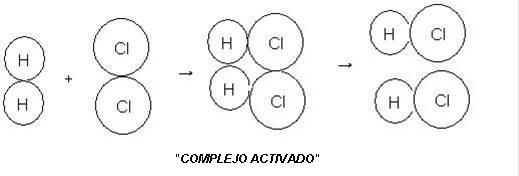
Colisión Vertical
Factores que modifican la velocidad de una reacción :
-Concentración de reactivos
- Temperatura
- Naturaleza de los reactivos
- Uso de catalizadores
Factores que modifican la velocidad de las reacciones Para que dos sustancia reaccionen, sus moléculas, átomos o iones deben chocar. Estos choques producen un nuevo ordenamiento electrónico y, por consiguiente un nuevo ordenamiento entre sus enlaces químicos, originando nuevas sustancias.
Temperatura
Por norma general, la rapidez de reacción aumenta con la temperatura porque al aumentarla incrementa la energía cinética de las moléculas. Con mayor energía cinética, las moléculas se mueven más rápido y chocan con más frecuencia y con más energía. El comportamiento de la constante de rapidez o coeficiente cinético frente a la temperatura = lnA − (Ea / R)(1 / T2 − 1 / T1) esta ecuación linealizada es muy útil y puede ser descrito a través de la Ecuación de Arrhenius K= Aexp( − EA / RT) donde K es la constante de la rapidez, A es el factor de frecuencia, EA es la energía de activación necesaria y T es la temperatura, al linealizarla se tiene que el logaritmo neperiano de la constante de rapidez es inversamente proporcional a la temperatura, como sigue: ln(k1 / k2) la hora de calcular la energía de activación experimentalmente, ya que la pendiente de la recta obtenida al graficar la mencionada ley es: -EA/R, haciendo un simple despeje se obtiene fácilmente esta energía de activación, tomando en cuenta que el valor de la constante universal de los gases es 1.987cal/K mol. Para un buen número de reacciones químicas la rapidez se duplica aproximadamente cada diez grados centígrados.




Estado Físico de los Reactivos
Si en una reacción interactúan reactivos en distintas fases, su área de contacto es menor y su rapidez también es menor. En cambio, si el área de contacto es mayor, la rapidez es mayor.
Al encontrarse los reactivos en distintas fases aparecen nuevos factores cinéticos a analizar. La parte de la reacción química, es decir, hay que estudiar la rapidez de transporte, pues en la mayoría de los casos estas son mucho más lentas que la rapidez intrínseca de la reacción y son las etapas de transporte las que determinan la cinética del proceso.
No cabe duda de que un mayor área de contacto reduce la resistencia al transporte, pero también son muy importantes la difusividad del reactivo en el medio, y su solubilidad, dado que esta es el límite de la concentración del reactivo, y viene determinada por el equilibrio entre las fases.


Presencia de un catalizador
Los catalizadores aumentan o disminuyen la rapidez de una reacción sin transformarse. Suelen empeorar la selectividad del proceso, aumentando la obtención de productos no deseados. La forma de acción de los mismos es modificando el mecanismo de reacción, empleando pasos elementales con mayor o menor energía de activación.
Existen catalizadores homogéneos, que se encuentran en la misma fase que los reactivos (por ejemplo, el hierro III en la descomposición del peróxido de hidrógeno) y catalizadores heterogéneos, que se encuentran en distinta fase (por ejemplo la malla de platino en las reacciones de hidrogenación).
Los catalizadores también pueden retardar reacciones, no solo acelerarlas, en este caso se suelen conocer como retardantes o inhibidores, los cuales impiden la producción.
Concentración de los reactivos
La mayoría de las reacciones son más rápidas en presencia de un catalizador y cuanto más concentrados se encuentren los reactivos, mayor frecuencia de colisión.
La obtención de una ecuación que pueda emplearse para predecir la dependencia de la rapidez de reacción con las concentraciones de reactivos es uno de los objetivos básicos de la cinética química. Esa ecuación, que es determinada de forma empírica, recibe el nombre de ecuación de rapidez. De este modo si consideramos de nuevo la reacción hipotética la rapidez de reacción "r" puede expresarse como ![r = k[A]^{m}[B]^{n} \,\!](http://upload.wikimedia.org/math/d/7/2/d721257f573e003e652dfc0695d96a1f.png) Los términos entre corchetes son las molaridades de los reactivos y los exponentes m y n son coeficientes que, salvo en el caso de una etapa elemental no tienen por que estar relacionados con elcoeficiente estequiométrico de cada uno de los reactivos. Los valores de estos exponentes se conocen como orden de reacción.
Los términos entre corchetes son las molaridades de los reactivos y los exponentes m y n son coeficientes que, salvo en el caso de una etapa elemental no tienen por que estar relacionados con elcoeficiente estequiométrico de cada uno de los reactivos. Los valores de estos exponentes se conocen como orden de reacción.
![r = k[A]^{m}[B]^{n} \,\!](http://upload.wikimedia.org/math/d/7/2/d721257f573e003e652dfc0695d96a1f.png) Los términos entre corchetes son las molaridades de los reactivos y los exponentes m y n son coeficientes que, salvo en el caso de una etapa elemental no tienen por que estar relacionados con elcoeficiente estequiométrico de cada uno de los reactivos. Los valores de estos exponentes se conocen como orden de reacción.
Los términos entre corchetes son las molaridades de los reactivos y los exponentes m y n son coeficientes que, salvo en el caso de una etapa elemental no tienen por que estar relacionados con elcoeficiente estequiométrico de cada uno de los reactivos. Los valores de estos exponentes se conocen como orden de reacción.
es una información muy agradable e interesante que permite el conocimiento de la cinética química
ResponderEliminar